Az SMA patológiája
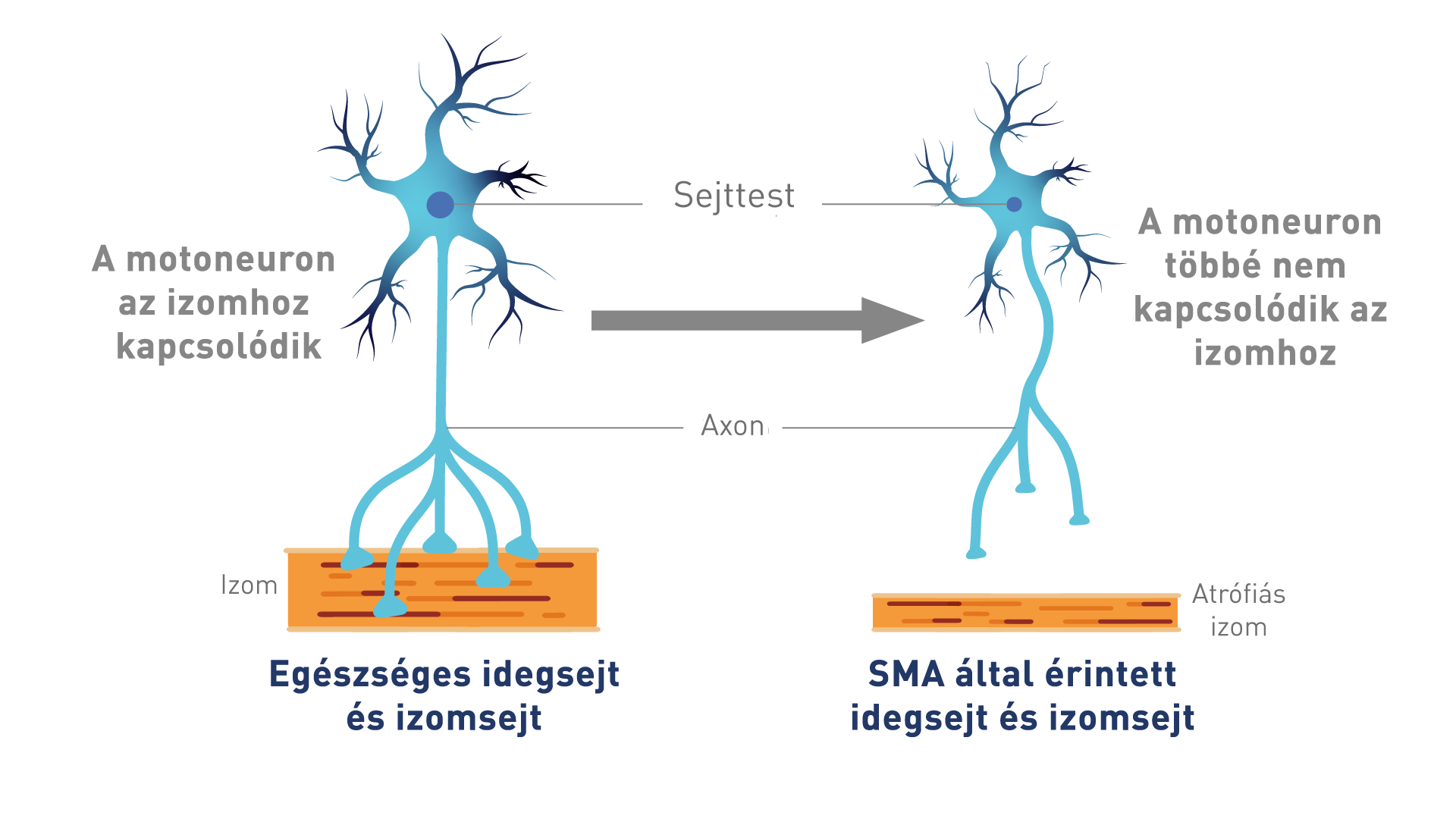
A gerincvelői izomsorvadás (spinal muscular atrophy, SMA) egy neuromuszkuláris betegség, amelyet a gerincvelőben lévő motoneuronok degenerációja okoz1. SMA esetén a túlélő motoneuron (survival motor neuron, SMN) fehérje hibás, aminek a hátterében az SMN1 gén deléciója vagy mutációja áll1. Az SMN-fehérje elégtelen mennyisége miatt a motoneuronok működésében zavar támad és a sejtek elpusztulnak, ami izomgyengeséget és atrófiát eredményez1.
Az SMA öröklődése
Az SMA egy autoszomális recesszív betegség1. Ennélfogva ahhoz, hogy egy gyermeknél SMA alakuljon ki, mindkét szülőjétől örökölnie kell egy-egy delécióval érintett (hiányzó) vagy mutáns SMN1 gént. Azok, akik csak egy hiányzó vagy mutáns SMN1 gént örökölnek, hordozni fogják a betegséget, vagyis egészségesek lesznek, de születő utódaik lehetséges, hogy SMA-val érintettek lesznek.
Azok a gyermekek, akiknek mindkét szülője hordozza az SMA-t, 50%-os eséllyel lesznek maguk is hordozók és 25%-os eséllyel fog kialakulni náluk az SMA2. Ötvenből körülbelül 1 személy hordozza az SMA-t3.

SMN1 és SMN2
Az SMN-fehérjének nem a teljes mennyisége képződik az SMN1 génről: valamennyi fehérje az SMN2-ről is készül. Az egészséges emberekben és az SMA-val élőkben legalább egy kópiája megtalálható a tartalék génnek, az SMN2-nek, amely szerkezetileg ugyan hasonlít az SMN1-hez, a róla képződött fehérjének csupán a 10%-a teljesen működőképes4. Az SMN2 gén kópiaszáma egyénenként eltérő1, így a tartalék fehérje mennyisége is változó.
Mindkét gén az 5q kromoszómán helyezkedik el1.
SMN1 gén: Túlélő motoneuron 1 gén1, 4
- A teljes hosszúságú, működőképes SMN-fehérje elsődleges forrása.
- Az SMA-val élőkben nem tud működőképes fehérje képződni az SMN1 génről.
- Ha nincs elég SMN-fehérje, a motoneuronok és a kapcsolódó izomsejtek túlélése ellehetetlenül.
SMN2 gén: Túlélő motoneuron 2 gén1, 4
- A kópiaszámok egyénenként eltérőek.
- Mindössze 5 építőelemben különbözik az SMN1-től.
- A termelt fehérjének csak körülbelül a 10%-a teljesen működőképes.
- Az SMA-val élők számára ez az SMN-fehérje egyetlen forrása.
- A kópiaszám általában fordítottan arányos az SMA súlyosságával.

Az SMA incidenciája és prevalenciája
Az SMA összesített prevalenciája 100 000 emberből 1-2, és 100 000 élve születésből körülbelül 8 új eset fordul elő3. Az SMA incidenciája és prevalenciája a típustól függően változó: az 1-es típus, ami a legsúlyosabb forma, az esetek 60%-át teszi ki3.
Az SMA típusai
A betegeket a tünetek első kialakulása alapján sorolják SMA-típusokba – minél korábban jelennek meg, annál súlyosabb a betegség progressziója5. A típusok közötti határok képlékenyek és gyakran nehéz különbséget tenni. Ezért a betegeket alternatív módon az „ülni nem képesek”, „ülni képesek” vagy „járni képesek” csoportjába sorolják6.
| SMA-típus | 1-es típus | 2-es típus | 3-as típus |
|---|---|---|---|
| SMN2 génkópiák jellemző száma | 2 | 3 | 3 vagy 4 |
| Életkor a betegség kialakulásakor | 0-6 hónap | 7-18 hónap | > 18 hónap |
| Maximálisan elért motoros képességek | Csak segítséggel képes ülni | Önállóan képes ülni | Tud járni |
| Várható élettartam terápia nélkül | < 2 év | Kb. 70%-os túlélés 25 éves korig | Normális |
| lncidencia 100 000 főre vetítve | 6 | 0.9 - 5.3 | 0.5 - 4.6 |
| Ülni nem képes betegek | Ülni képes betegek | Járni képes betegek |
|---|---|---|
| Sosem tudott önállóan ülni vagy elveszítette ezt a képességét (túlnyomórészt 1-es és 2-es típus) | Önállóan képes ülni több mint 10 másodpercig (2-es és 3-as típus, valamint kezelt 1-es típusú betegek) | Önállóan járva megtesz több mint 10 métert (3-as típus, kezelt, tüneteket még nem mutató betegek) |
A betegség tipikus jelei
Az SMA spektruma széles, a tünetek pedig egyénenként változóak1, 5, 9. Az egyes ismertetett tünetek akármelyik típusban előfordulhatnak.
1-es típus5, 10, 11:
| Tünet megjelenése |
|
|---|---|
| A motoros fejlődés fő állomásai |
|
| Betegségteher |
|
2-es típus5, 10, 11:
| Tünet megjelenése |
|
|---|---|
| A motoros fejlődés fő állomásai |
|
| Betegségteher |
|
3-as típus5, 10, 11:
| Tünet megjelenése |
|
|---|---|
| A motoros fejlődés fő állomásai |
|
| Betegségteher |
|
Diagnózis
Az SMA tünetei
Az SMA-nak sokféle tünete van, amelyek nem kizárólag a vázizmokat érintik1. Egyidejűleg fennálló betegségek is előfordulhatnak, amelyek meglehetősen nagy változatosságot mutathatnak a betegek körében1, 2. Ezek súlyosan kihathatnak a beteg életminőségére3.
Az SMA a kognitív funkciókat és az intelligenciát nem érinti hátrányosan4.
- Köhögés nehezítettsége
- Kiújuló fertőzések
- Hipoventiláció (csökkent légzés) alvás közben
- A mellkasfal és a tüdő alulfejlettsége
- Tüdőelégtelenség
- Csökkent vitálkapacitás
- Légszomj intenzív testmozgás közben
- Csonttörések
- Osteopenia (csökkent csontsűrűség)
- A csontozat deformitásai (gerincferdülés, csípőficam)
- Kontraktúra (merevség), főként a kéz és a lábfej ízületeiben
Az egyidejűleg fennálló légzési, táplálkozási és mozgásszervi zavarok kezelése érdekében specialistákat is be kell vonni, színesítve a multidiszciplináris csapatot1, 5, 6, 8
Az SMA progressziója
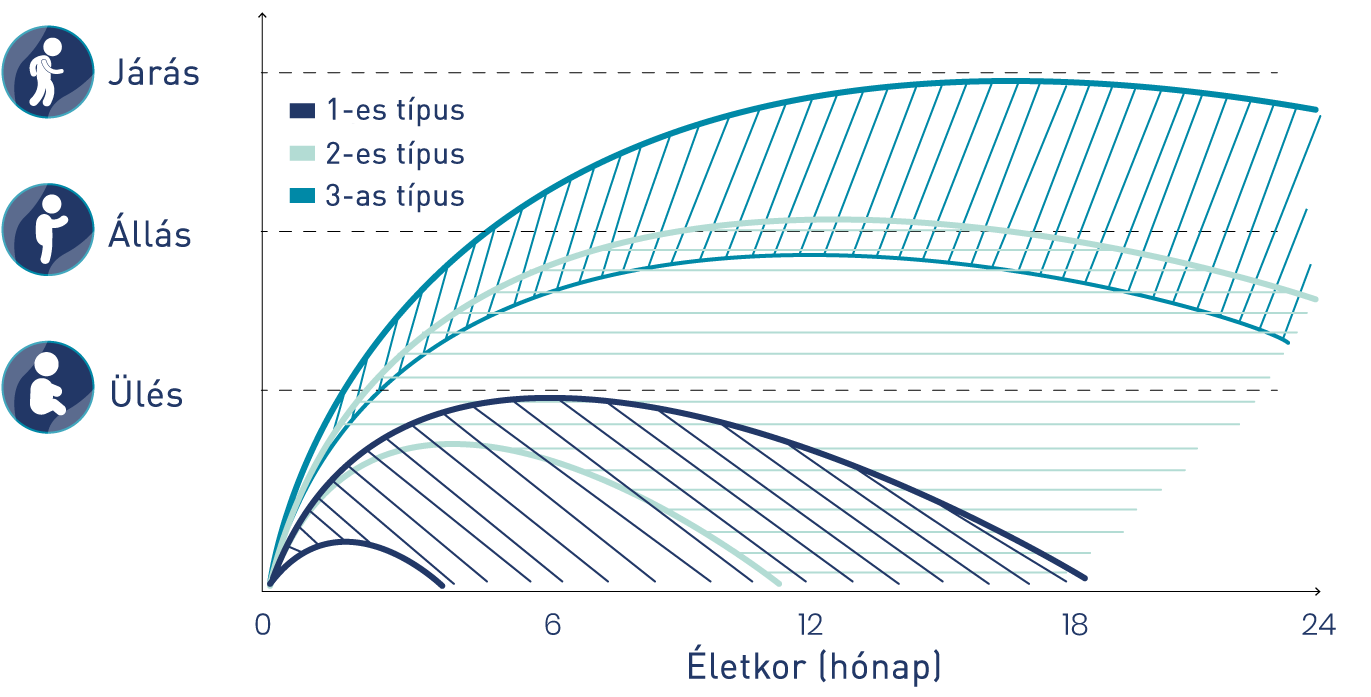
Az SMA természetes lefolyását az SMA mindegyik típusa esetén, minden korcsoportban az izomgyengeség fokozódása és a megszerzett motoros funkciók elvesztése jellemzi. A motoros képességek elvesztése különböző életkorokban, különböző gyorsasággal történhet2. Az alábbi grafikon a kezeletlen SMA-betegek természetes betegségprogresszióját szemlélteti.
Kezelési lehetőségek
A kezelés várt hatása
Az SMA jelenleg nem gyógyítható. A jelenlegi kezelések a betegség progressziójának lassitására, valamint a motoros funkciók és az életminőség stabilizálására és javítására irányulnak. Gyermekek esetében a várható élettartam megnövelése is a fontos terápiás célok között szerepel.1, 2
Egy 2019-ben végzett európai felmérésben az SMA-val élő betegek (SMA 1–4-es típus) vagy gondozóik 96,6%-a úgy nyilatkozott, hogy egy olyan kezelést, amely stabilizálja a betegség lefolyását, sikeresnek tekintenének3. Egy másik, felnőtt 2-es és 3-as típusú betegek körében végzett felmérésben a betegek az alábbiakat jelölték a legfontosabb megőrzendő és javítandó4 képességeknek.
 A három legfontosabb javítandó képesség4:
A három legfontosabb javítandó képesség4:

Az SMA betegek gondozása
A betegség jelentős hatásai miatt az optimális orvosi csapat nem csupán egyetlen orvosi szakterületet ölel fel, hanem a betegség által érintett különböző területekre specializálódott szakemberek széles skáláját foglalja magában5, 6, 7, 8.
Interdiszciplináris megközelítés: A kezelés interdiszciplináris megközelítésének célja, hogy a lehető legtovább megőrizze a beteg mobilitását és önállóságát, lehetővé téve számára a részvételt a társas és munkával kapcsolatos tevékenységekben5, 6, 7, 8.
Proaktív gondozás: A cél az életminőség orvosi beavatkozások révén való javítása. Ez magában foglalhatja az adott betegre szabott légzés- és táplálkozási támogatást, valamint ortopédiai segédeszközök és gyógytorna biztosítását.
Kezelési lehetőségek
Az SMA-t a SMN-fehérje elégtelen mennyisége okozza, ami a motoneuronok pusztulásához vezet, továbbá izomgyengeséget és atrófiát eredményez9.
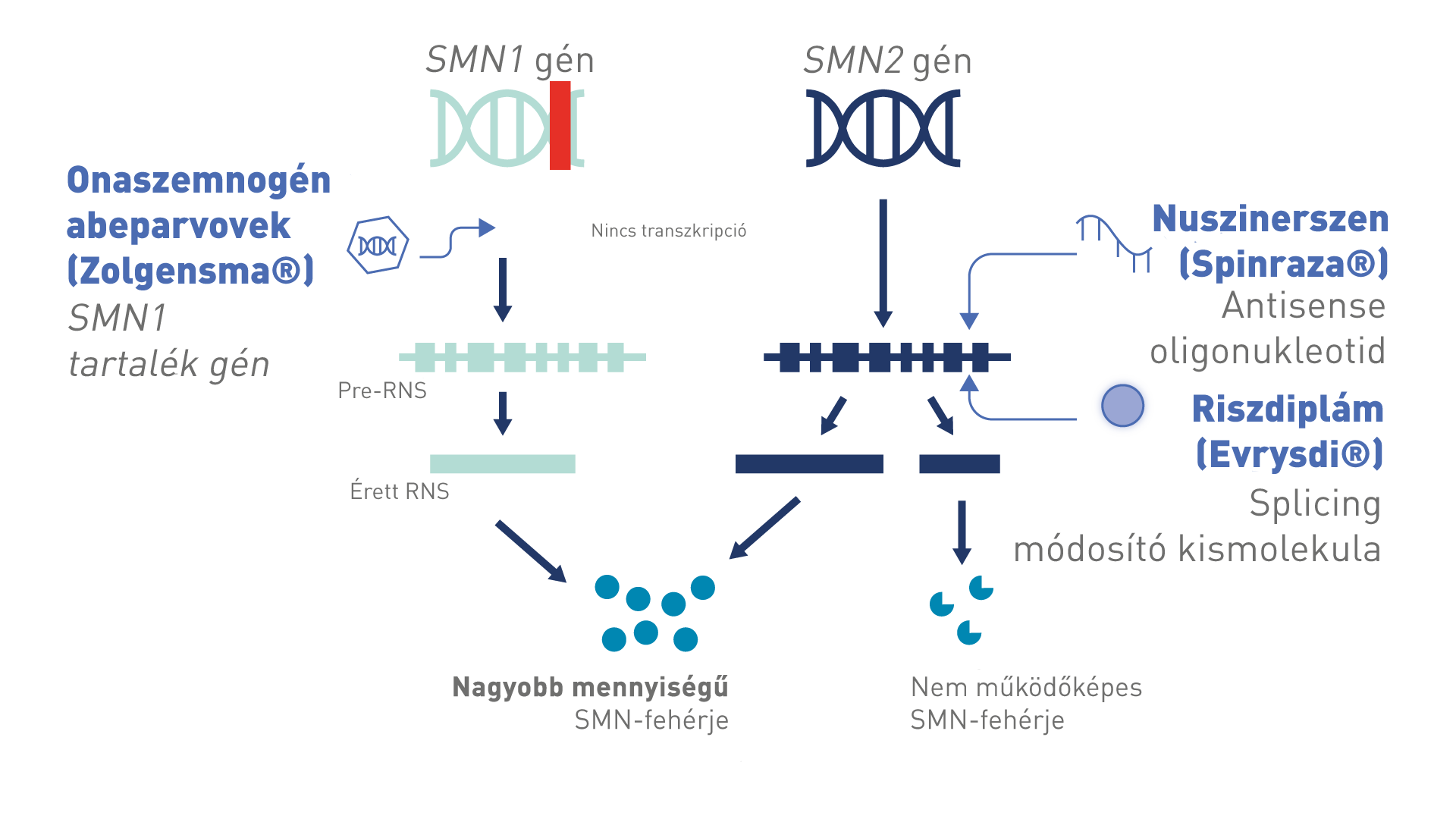
2024. júliusáig az SMA kezelésére 3 gyógyszerkészítményt hagyott jóvá az Európai Gyógyszerhatóság: a nuszinerszent (Spinraza®)10, a riszdiplámot (Evrysdi®)11 és az onaszemnogén abeparvoveket (Zolgensma®)12.
Mindhárom kezelés az SMN-fehérje termelődését fokozza. A nuszinerszen és a riszdiplám esetében ezt az SMN2 pre-RNS-ének splicingját javítva érik el10, 11 (a Spinraza® hatásmechanizmusával kapcsolatban további részletek a Spinraza®/nuszinerszen áttekintése nevű lapra kattintva érhetők el). Az onaszemnogén abeparvovek egy vírusvektoron keresztül juttatja be a működőképes SMN1 gént a sejtekbe12.
A kezelés kiválasztása
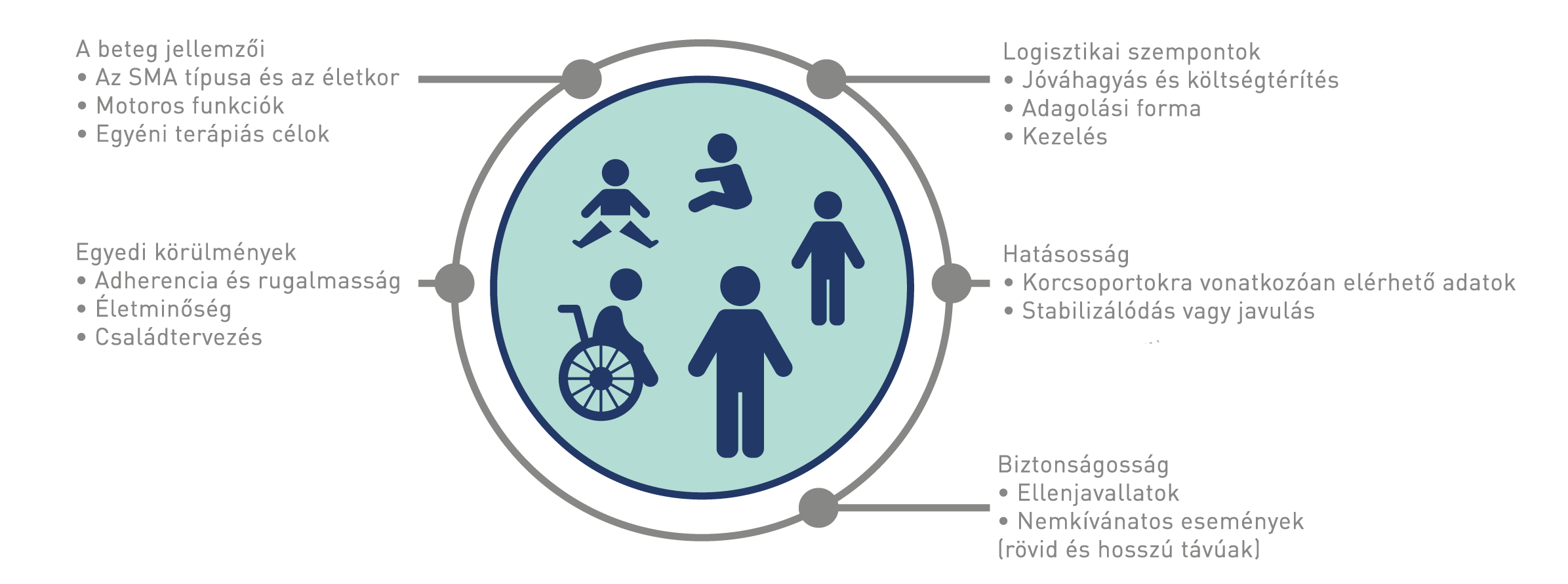
Az SMA-betegeknek számos terápiás lehetőség áll a rendelkezésére10, 11, 12.
A javallat megállapításához és a költségek fedezéséhez az orvosoknak általában a klinikai megjelenés alapján meg kell határozniuk az SMA típusát, valamint genetikai laboratóriumi elemzés révén az SMN1 mutációjának típusát és az SMN2 kópiaszámát 10, 11, 12, 13, 14, 15.
| Jóváhagyás* | A genetikai eredetű SMA kezelésére javallott | |
|---|---|---|
| Nuszinerszen10 | 201716 | Nincs életkori korlátozás.Az 5q kromoszómához kötött spinalis izomatrophia kezelésére javallott. |
| Riszdiplám11 | 202117, | Nincs életkori korlátozás† .Az 5q spinalis muscularis izomatrophia (SMA) kezelésére javallott olyan betegeknél, akinél 1-es, 2-es vagy 3-as típusú SMA klinikai diagnózist állítottak fel vagy egy-négy SMN2-kópia megléte esetén. |
| Onaszemnogén abeparvovek12 | 202118 |
Javallott:
|
†A < 16 naposnál fiatalabb életkorra vonatkozóan nincsenek adatok. *A Swissmedic által Svájcban adott jóváhagyás ideje. #Az SMN1 gén mindkét kópiájának mutációja vagy deléciója.
Alkalmazás
A nuszinerszennek, a riszdiplámnak és az onaszemnogén abeparvoveknek eltérő az alkalmazási módja és a kezelési rendje10, 11, 12. A terápiaváltás korlátozott mértékben, de lehetséges.

Gyógyszerbiztonság
Nagyon gyakori (≥1/10 a gyakorisági konvenció szerint) mellékhatások, amelyek előfordulhatnak az SMA-terápiák mellett:
Onaszemnogén abeparvovek12
Májenzimek emelkedett szintjeEzek a mellékhatások a post-lumbalpunctiós szindróma megnyilvánulási formáinak tekinthetők.10.
Az onaszemnogén abeparvovekkel végzett kezelés után a májfunkciót (ALT, AST, totál bilirubin) az infúzió beadása után még legalább 3 hónapig figyelni kell, ha klinikailag javallott, akkor még tovább12.
A kezelést minden SMA-beteg esetében egyénileg kell megválasztani19, 20, 21, 22.
A nuszinerszen (Spinraza®) áttekintése
A nuszinerszen segít a szervezetnek több működőképes SMN-fehérjét termelni azáltal, hogy fokozza az SMN2 génről történő fehérjetermelést1:
Hatásmechanizmus
Milyen gyógyszer a nuszinerszen?
A nuszinerszen az antisense oligonukleotidok nevű gyógyszercsoportba tartozik. Ezek egyszálú nukleotidláncok (amelyek a DNS-hez és RNS-hez hasonló alkotóelemekből épülnek fel), amelyek egy cél-RNS-hez kötődnek és ezáltal módosítják: csökkentik vagy fokozzák a fehérjetermelést2.
Mi a baj az SMN2 génnel, és hogyan segíthet a nuszinerszen?
Az SMN2 génről képződött fehérjék többsége nem működőképes, és gyorsan lebomlik. A nuszinerszen kapcsolatba lép az SMN2 gén úgynevezett pre-mRNS-ével és elősegíti a működőképes SMN-fehérje termelődését1. Ez a terápiás módszer visszafordítható és nem vezet a genetikai kód módosulásához3

* A mellkasi gerincvelő elülső szarvának post mortem képelemzése szerint a kezelt betegeknél (n=3) jelentősen nagyobb volt a neuronokban található SMN-fehérje mennyisége (p<0,0001), mint a nem kezelt betegeknél (n=2).16
Milyen hatást gyakorol a sejtekre?
Az SMN-fehérje szintjének növekedése az idegsejtekben elejét veszi ezen sejtek további pusztulásának, és ezáltal megakadályozza a betegség progresszióját és a tünetek rosszabbodását. A súlyosságtól függően az izomműködés akár még javulhat is a terápia hatására11.
Alkalmazás
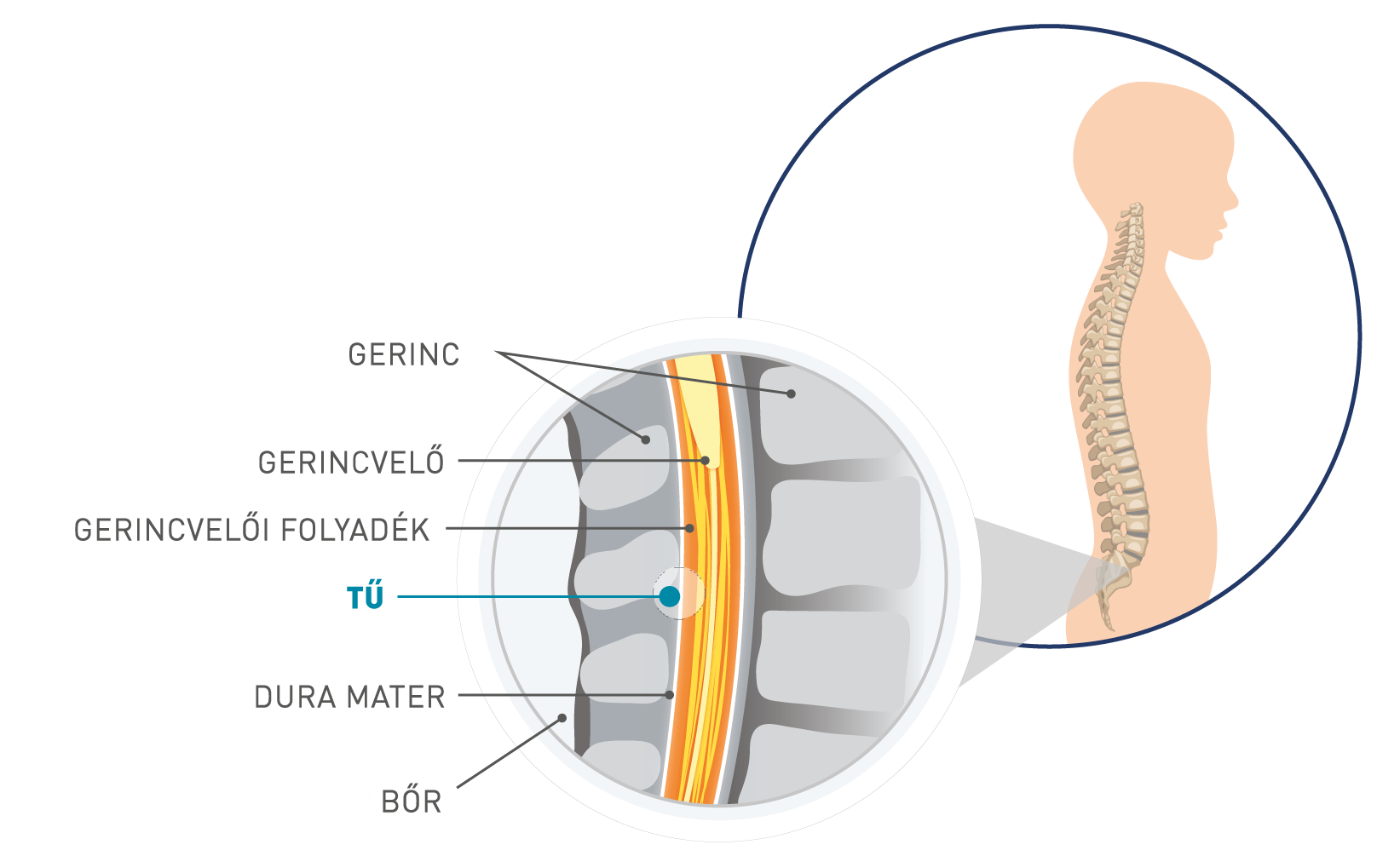
A nuszinerszent injekcióval juttatják be az alsó gerinccsatornába – ezt az eljárást lumbálpunkciónak vagy intratekális injekciónak nevezik1. Végezhető ultrahang vagy más képalkotó technika segítségével is, különösen akkor, ha a betegnél scoliosis (gerincferdülés) van jelen vagy ortopédiai eszközöket visel5.
A lumbálpunkció lehetővé teszi, hogy a hatóanyag nagy koncentrációban jusson el oda, ahová kell. Ezek a nagy koncentrációk viszonylag alacsony dózisokban érhetők el, ami minimalizálja a mellékhatásokat6.
Az otthon alkalmazandó gyógyszerekkel ellentétben ez a terápiás módszer jobb adherenciát és a motoros funkciók jobb nyomon követését teszi lehetővé7
A kezelés négy kezdő, a 0., 14., 28. és 63. napon beadandó telítő adagot foglal magában, amelyeket négyhavonta adott fenntartó adagok követnek1

Eredmények
A nuszinerszen hatásosságát és biztonságosságát egy széles körű klinikai programban vizsgálták, amely egy széles betegpopulációt foglalt magában8, 9, 10, 11, 12
A vizsgálatok az alábbiakat foglalták magukban:
- A kezelés elkezdésekor különböző életkort betöltött résztvevők, az újszülöttektől a serdülőkig
- 1–3-as típusú SMA
- Tünetes és tüneteket még nem mutató betegek
A klinikai vizsgálati adatokon kívül a nuszinerszen hatékonyságát valós körülmények között, széles és heterogén betegpopulációkból származó bizonyítékok is igazolják. Egy, a klinikai gyakorlatban végzett metaanalízis a motoros funkciók javulását tárta fel olyan 2-es és 3-as típusú SMA-val élő betegeknél, akik 0–14 hónapon keresztül nuszinerszent kaptak, és kezeletlen betegekkel hasonlították össze őket. Az eredmények szerint a nuszinerszen jelentősen javította a HFMSE-pontszámmal mért motoros funkciókat13.

*A betegek számát és életkorát, valamint az országok számát 30 vizsgálat adatainak felhasználásával számoltuk ki. †Összesített átlagos különbség a kiindulástól számított 10–24 hónapon keresztül, random hatás modellel becsülve. A vizsgálatok közötti heterogenitást az I2 együtthatóval számszerűsítettük.‡I2 = 90.0%. §I2 = 81.0%. ¶I2 = 88.6%.
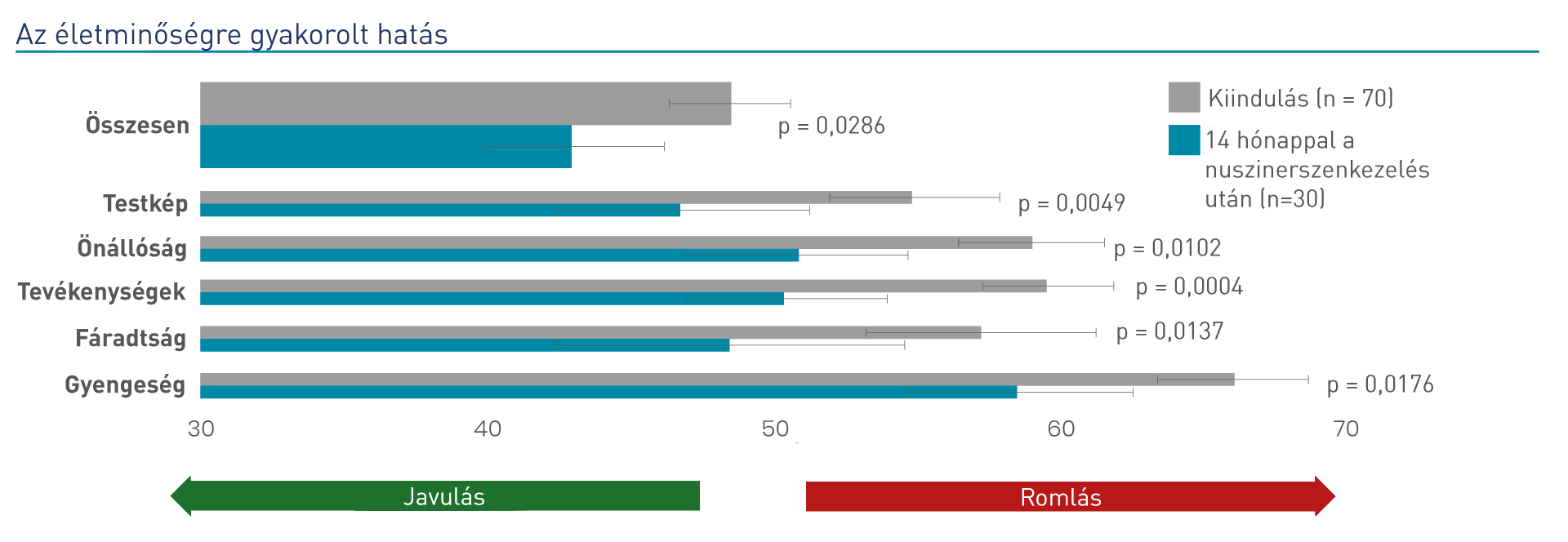
Egy másik vizsgálat a nuszinerszennel végzett kezelés életminőségre gyakorolt hatását vizsgálta 78 olyan felnőtt SMA-beteg körében, akiket 14 hónapon át nuszinerszennel kezeltek. Az (INQoL) egyénre szabott neuromuszkuláris életminőségi skálát alkalmazva javulást figyeltek meg mind az összpontszám, mind a 7 egyéni domén tekintetében, amelyek a következők voltak: testkép, önállóság, tevékenységek, fáradtság, gyengeség, társas kapcsolatok és érzelmek14.
Az életminőség globális pontszáma nem korrelált a HFMSE- vagy RULM-pontszámokkal. Ez azt jelzi, hogy az életminőség értékelését kiegészítő mérésként kellene alkalmazni az SMA értékelése során14.
Biztonságosság
A biztonságossági információkat lásd a Gyógyszerbiztonság című részben.
Összefoglalás

A hatás helyére történő, célzott beadás, amely képes csökkenteni az egész szervezetben (szisztémásan) fellépő mellékhatások kockázatát6.

Hatásosságát kiterjedt klinikai vizsgálatok és a klinikai gyakorlat adatai bizonyítják1, 8, 9, 10, 11, 12, 13, 14.

A motoros fejlődés fő állomásainak lehetséges elérése és a motoros funkciók - nagyban az életkornak megfelelő - fejlődése a tüneteket egyelőre nem mutató betegeknél11.

A motoros funkciók stabilizálódása/javulása SMA 2-es és 3-as típusú betegeknél13.

Az életminőség javulása felnőtt SMA-betegeknél14.


A SPINRAZA® az 5q kromoszómához kötött gerincvelői izomsorvadás kezelésére javallott.
Spinraza 12 mg oldatos injekció
Hatóanyag: nuszinerszen. Orvosi rendelvényhez kötött gyógyszer (Sz, Ú).
Bővebb információért olvassa el a gyógyszer teljes alkalmazási előírását! A hatályos alkalmazási előírás teljes szövegét megtalálja az NNGYK honlapján. Elérési útvonal: https://ogyei.gov.hu/gyogyszeradatbazis oldalon a termék nevére keresve, a keresési eredmény „törzskönyvezési státusz” oszlopában található kék nyílra kattintva elérhetők a gyógyszerkészítényre vonatkozó alapadatok. Itt a „kísérőiratok” linkre kattintva megnyílik a készítmény magyar nyelvű alkalmazási előírása (https://www.ema.europa.eu/documents/product-information/spinraza-epar-product-information_hu.pdf).
Ártámogatás: nem támogatott készítmény.
További információ: Biogen Hungary Kft. 1113 Budapest, Bocskai út 134-146. E/2; Tel.: +36 1 8 999 880
Biogen-246277
Lezárás dátuma: 2024. Október
